「在全球頂尖腫瘤學術年會上報告、在國際權威期刊上發表、推動國產新藥獲批上市,HARMONi-A研究在科學性和實用性上取得的‘三連響’,彰顯了‘中國學者+本土新藥’組合的強勁實力,展示了國際學術界對國產首創雙抗新藥方案的認可。」中山大學腫瘤防治中心內科主任張力教授說。
5月31日,張力教授牽頭開展的III期HARMONi-A(AK112-301)研究期中分析結果被2024年美國臨床腫瘤學會(ASCO)收錄為口頭報告,由張力教授在ASCO會上做口頭報告。研究結果同步被國際頂尖權威期刊【美國醫學會雜誌】(JAMA)線上發表。

張力教授在2024ASCO會上做口頭報告。
這是首個比較了依禾菲單抗聯合化療與單獨化療在EGFR-TKI耐藥的EGFR突變晚期或轉移性nsq-NSCLC療效的雙盲、安慰劑對照、隨機的III期研究。研究結果顯示, 「依禾菲單抗聯合化療」突破EGFR-TKI治療後耐藥的臨床困境,為EGFR-TKI耐藥的非小細胞肺癌患者帶來全新的標準治療方案 。6月17日,張力教授團隊接受采訪,向媒體介紹了這一治療新方案的諸多亮點。

解決耐藥問題
新方案主要攻克三大難點
數據顯示,2022年,中國肺癌新發病例數為106.06萬人,死亡病例高達73.33萬人。在中國肺癌患者中,非小細胞肺癌患者占比約85%,其中EGFR突變陽性的占比高達50%。針對這部份EGFR突變非小細胞肺癌患者,靶向治療方式EGFR-TKI是標準一線治療,但獲得性耐藥不可避免。目前臨床上EGFR-TKI尤其是第三代TKI治療進展患者,最佳的治療選擇仍然有限。
據研究團隊成員、中山大學腫瘤防治中心內科主任醫師、教授方文峰介紹,當患者出現耐藥後,含鉑雙藥化療仍是最主要的治療手段,但仍存在明顯不足:客觀有效率(ORR)大約只有25%-40%;平均腫瘤控制時間(PFS)僅為4-5個月;平均生存時間(OS)約為14-20個月。
方文峰教授表示,為了解決患者的耐藥問題,治療方案需要攻克三大難點:
首先,根據腫瘤突變負荷低、抗原雜問題,可以透過化療、放療把腫瘤細胞的抗原暴露出來,讓免疫細胞找到它;
其次,由於EGFR突變非小細胞肺癌屬於冷腫瘤,腫瘤中的免疫細胞少,透過抗血管生存可以增加免疫細胞對腫瘤的浸潤,改善腫瘤缺氧和腫瘤免疫微環境抑制狀態;
最後,腫瘤細胞的PD-L1蛋白,會誘導免疫細胞上高表達PD-1。二者結合,就會抑制免疫細胞的功能,幫助腫瘤逃脫免疫查殺。要透過PD-1/PD-L1抗體或雙免疫阻止二者的結合。
此次張力教授團隊采用的依禾菲單抗由中國藥企康方生物研發,具有抗PD-1/VEGF-A雙抗,有望以「一藥雙靶」一次解決上述三大問題中的後兩大問題。
2021年11月,張力教授牽頭的III期HARMONi-A研究在中國啟動,全國55個研究中心共納入322例EGFR-TKI治療失敗的非小細胞肺癌,隨機(1:1)接受依禾菲單抗(n=161)或安慰劑(n=161)聯合培美曲塞+卡鉑Q3W 4個周期治療,隨後接受依禾菲單抗+培美曲塞或安慰劑+培美曲塞的維持治療。主要終點是根據RECISTv1.1標準由獨立放射學評審委員會(IRRC)評估的意向治療(ITT)人群的無進展生存期(PFS)。
據介紹,研究中有86%的患者接受了第三代EGFR-TKI治療,依禾菲單抗聯合治療組和化療組分別有86.3%和85.1%,腦轉移患者分別有21.7%和23.0%。
經過近3年的多中心雙盲、安慰劑對照、隨機的III期研究,HARMONi-A研究呈現出令業界驚喜的結果。
延長無進展生存期
疾病進展或死亡風險降低54%
據方文峰教授介紹,截至2023年3月10日,中位隨訪時間為7.89個月,期中分析結果顯示,依禾菲單抗聯合方案相比化療可顯著延長患者無進展生存期(PFS),無進展生存期從單獨化療的4.8個月,提升至7.06個月。風險比(HR)為0.46,降低疾病進展或死亡風險達54%。
依禾菲單抗聯合化療在3個月(94.7%對69.7%)、6個月(55.4%對33.1%)和9個月(37.9%對18.3%)的無進展生存期率均高於單獨化療。
「我們如何理解這個數碼?簡單來說,9個月時,約82%的單純化療患者已經出現疾病進展,而依禾菲聯合化療組還有約38%的患者仍在接受治療中。」張力教授說。
亞組分析顯示,在接受第三代EGFR-TKI治療失敗、基線有腦轉移、EGFR突變為19號外顯子缺失以及T790M突變陽性的患者亞組中,依禾菲單抗聯合方案均顯示出無進展生存期獲益優勢。
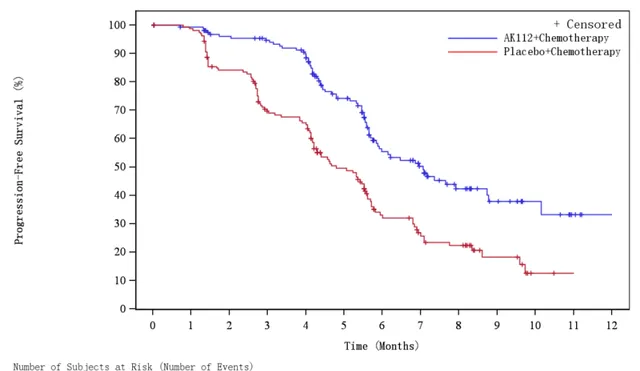
意向治療人群(ITT)的無進展生存期。其中藍線為依禾菲聯合化療組,紅線為單獨化療組。
依禾菲單抗聯合化療對比化療組的客觀緩解率(ORR)為50.6%和35.4%。截至2023年12月,中位隨訪時間為17.6個月,依禾菲聯合方案中位總生存期為17.1個月,對照組中位生存期為14.5個月,降低死亡風險20%。敏感性分析顯示,依禾菲單抗聯合方案組觀察到生存期有明顯延長趨勢,降低死亡風險23%。

OS生存曲線圖。其中藍線為依禾菲聯合化療組,紅線為單獨化療組。
研究結果表明,HARMONi-A方案整體安全可控,兩組間常見不良反應發生率無明顯差異。兩組的治療期間出現的不良反應(TEAE)發生率分別為61.5%和49.1%,其中最常見的為化療相關不良事件。≥3級免疫相關不良事件(irAE)發生率分別為6.2%和2.5%;≥3級VEGF相關不良事件發生率為3.1%和2.5%。
展示 「 中國學者+本土新藥 」 組合實力
新藥有望進入醫保談判
「2023年,我們研究團隊展開的依禾菲單抗聯合化療治療晚期非小細胞肺癌(NSCLC)的Ⅱ期臨床研究結果在柳葉刀旗下子刊eClinicalMedicine發表。當時這個實驗結束後,我們發現了這個藥物的特色,主動聯系了康方生物希望開展III期研究。」張力教授表示,「中國學者+本土新藥」的組合意味著中國對相關研究成果具有完整的自主知識產權。此次實驗促成全球首款PD-1/VEGF雙抗上市。在此前,張力教授團隊還曾助推全球首款雙抗ADC新藥出海。

據張力教授介紹,依禾菲單抗聯合化療用於經第三代EGFR-TKI治療進展的EGFR突變、局晚期或轉移性nsq-NSCLC的國際多中心III期HARMONi研究已經在高效開展中,研究結束後,有望在美國食品藥品監督管理局審批後上市。
今年5月,依禾菲單抗聯合化療治療EGFR-TKI治療進展的EGFR突變的局部晚期或轉移性nsq-NSCLC被國家藥品監督管理局(NMPA)批準上市。
「過去,很多新藥是由海外藥企研發,在經過海外學者試驗後,在海外首先上市,之後是中國批準上市。這款國產新藥是先在中國上市,再到海外進行實驗、爭取上市,整個過程彰顯了‘中國學者+本土新藥’組合的強勁實力。」據張力教授介紹,目前一次依禾菲單抗治療花費的價格在2萬元左右。因為該藥物在今年上半年獲批上市,很有希望進入醫保談判。
采寫:南都記者 王詩琪 通訊員 文朝陽 陳鋆 鄭敏珊
通訊員供圖











